發布時間: 2021-02-04
隨著醫學進步,目前乳癌患者的五年存活率已有90%。然而,一旦發生癌症轉移,存活率便會陡降到30%以下。因此,如何避免癌細胞的擴散,是現今乳癌治療的重點之一。
中央研究院基因體研究中心黃雯華助研究員團隊,近期發現並證實了一項乳癌惡化的機制。蛋白質DSG2(Desmoglein2)會隨著微環境的氧氣含量而增減,促使乳癌的增生與移轉。此研究首次觀察到癌症的蛋白質會動態變化,並影響癌症病程,未來可望幫助臨床診斷及治療。研究論文已於本(2021)年1月19日發表於《美國國家科學月刊》(PNAS)。
蛋白質DSG2原本常見於表皮細胞,負責細胞之間的黏附。2016年,黃雯華團隊在分析乳癌轉移的基因數據時,發現DSG2含量異常的高。經比對乳癌病患的檢體切片後也發現,癌細胞有DSG2的病患,存活率明顯偏低,並有較高的復發機率。同樣的現象,在以國外患者為族群的基因研究中也被證實,且不受限於乳癌的種類。
在動物實驗中,研究團隊將乳癌細胞植入小鼠乳腺脂肪袋,發現其乳癌細胞的DSG2基因表現量越高,小鼠的乳癌腫瘤就越大。不僅如此,其血液內以及轉移到肺臟的癌細胞也明顯較多。團隊進一步觀察發現,DSG2並非一直大量表現,而是會在特定階段中減少表現。此一改變,將使其成為癌症轉移的推手。
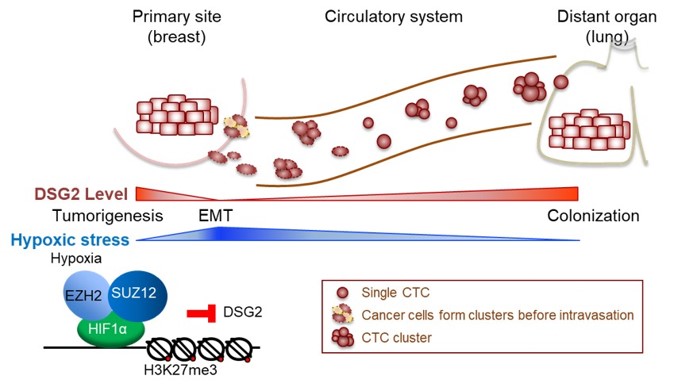
黃雯華解釋,癌細胞首先在乳房大量生長,並會藉由DSG2的黏附能力使腫瘤不斷增大。而當腫瘤核心的微環境開始出現缺氧的狀態時,另一種蛋白質──厭氧關鍵調節蛋白HIF-1α便會啟動反應:抑制DSG2。少了DSG2,癌細胞失去黏附力,開始脫離原生腫瘤、進入血液隨著循環系統傳播到體內其他部位,並生長成新腫瘤,形成癌轉移。
「值得注意的是,在有DSG2的小鼠體內,血液中的腫瘤細胞出現更多群聚移動的情況。」黃雯華推測,有DSG2的癌細胞有可能成群簇的從腫瘤邊緣剝落進入血液中,而DSG2也幫助這些血液中的癌細胞成團移動,比起單一癌細胞,更能在循環系統內存活下來,也更容易在其他組織附著、落地生根。
掌握DSG2的促癌機制,有助於將其作為癌症診斷的生物標記。黃雯華舉例,未來在臨床診斷上,可分析腫瘤中與血液中癌細胞的DSG2含量,以追蹤預後的表現,或檢視治療方法是否奏效。此外,也可以將DSG2作為治療標靶。然而,研究團隊也強調,相關治療策略的開發,仍須考量DSG2在癌症不同階段中的表現量及功能,有待癌症研究領域進一步探討。
事實上,不只有乳癌,許多數據也顯示子宮頸癌、頭頸癌和肺癌等也都有大量DSG2,且會影響預後情形,DSG2將有機會成為未來癌症研究關注的新焦點之一。除此之外,本研究另一項突破過去的發現,則是HIF-1α不僅會透過激活促癌基因使癌症惡化,有時還會藉由抑制其他促癌基因(如DSG2)的表現,加速腫瘤轉移。這也是相關領域未來值得留意的面向。
本研究由中研院及科技部支持,第一作者為張博皓博士後研究人員,黃雯華為通訊作者。其他參與者包含:陳吟詩、陳銘哲、蔡亞萍;臺大醫院病理科鄭永銘醫師、臺北榮總乳房醫學中心蔡宜芳醫師、臺北榮民總醫院腫瘤醫學部楊慕華醫師(提供乳癌檢體),以及國立臺灣海洋大學生科系許邦弘副教授(蛋白質譜分析)。研究論文:〈Interplay between desmoglein2 and hypoxia controls metastasis in breast cancer〉,全文詳見:https://www.pnas.org/content/118/3/e2014408118。
-
陳昶宏,中央研究院秘書處公關科
(02) 2789-8059,changhung@as.edu.tw
-
黃雯華助研究員,中央研究院基因體研究中心
(02) 2787- 1246, wendyhv@gate.sinica.edu.tw
-
郭姵君,中央研究院秘書處媒體小組
(02) 2789-8821,deartree@gate.sinica.edu.tw
-
相關連結









 首頁
首頁